Inden for moderne medicin har antibiotika vist sig at være en af de mest betydningsfulde fremskridt, idet de dramatisk har sænket forekomsten og dødeligheden forbundet med mikrobielle infektioner. Deres evne til at ændre de kliniske resultater af bakterieinfektioner har forlænget den forventede levetid for utallige patienter. Antibiotika er afgørende i komplekse medicinske procedurer, herunder operationer, implantatplaceringer, transplantationer og kemoterapi. Fremkomsten af antibiotikaresistente patogener har dog været en voksende bekymring, hvilket har mindsket effektiviteten af disse lægemidler over tid. Tilfælde af antibiotikaresistens er blevet dokumenteret på tværs af alle kategorier af antibiotika, efterhånden som mikrobielle mutationer opstår. Selektionspresset fra antimikrobielle lægemidler har bidraget til stigningen i resistente stammer, hvilket udgør en betydelig udfordring for den globale sundhed.
For at bekæmpe det presserende problem med antimikrobiel resistens er det afgørende at implementere effektive infektionskontrolpolitikker, der begrænser spredningen af resistente patogener, samtidig med at reducere brugen af antibiotika. Derudover er der et presserende behov for alternative behandlingsmetoder. Hyperbarisk iltbehandling (HBOT) er fremkommet som en lovende metode i denne sammenhæng, der involverer inhalation af 100 % ilt ved specifikke trykniveauer i en periode. HBOT, der er positioneret som enten en primær eller supplerende behandling af infektioner, kan give nyt håb i behandlingen af akutte infektioner forårsaget af antibiotikaresistente patogener.
Denne terapi anvendes i stigende grad som en primær eller alternativ behandling af forskellige tilstande, herunder inflammation, kulilteforgiftning, kroniske sår, iskæmiske sygdomme og infektioner. De kliniske anvendelser af HBOT i infektionsbehandling er omfattende og giver uvurderlige fordele for patienter.

Kliniske anvendelser af hyperbarisk iltbehandling ved infektion
Nuværende evidens understøtter robust anvendelsen af HBOT, både som en selvstændig og supplerende behandling, og giver betydelige fordele for inficerede patienter. Under HBOT kan det arterielle blodilttryk stige til 2000 mmHg, og den resulterende høje ilt-vævstrykgradient kan hæve vævets iltniveauer til 500 mmHg. Sådanne effekter er særligt værdifulde til at fremme helingen af inflammatoriske reaktioner og mikrocirkulationsforstyrrelser observeret i iskæmiske miljøer, samt til at håndtere kompartmentsyndrom.
HBOT kan også påvirke tilstande, der er afhængige af immunsystemet. Forskning tyder på, at HBOT kan undertrykke autoimmune syndromer og antigeninducerede immunresponser, hvilket hjælper med at opretholde transplantattolerance ved at reducere cirkulationen af lymfocytter og leukocytter, samtidig med at immunresponserne moduleres. Derudover kan HBOTunderstøtter helingved kroniske hudlæsioner ved at stimulere angiogenese, en kritisk proces for forbedret heling. Denne terapi fremmer også dannelsen af kollagenmatrix, en essentiel fase i sårheling.
Der skal lægges særlig vægt på visse infektioner, især dybe og vanskeligt behandlede infektioner såsom nekrotiserende fasciitis, osteomyelitis, kroniske bløddelsinfektioner og infektiøs endokarditis. En af de mest almindelige kliniske anvendelser af HBOT er til behandling af hud-bløddelsinfektioner og osteomyelitis forbundet med lave iltniveauer, der ofte er forårsaget af anaerobe eller resistente bakterier.
1. Diabetiske fodinfektioner
Diabetisk fodSår er en udbredt komplikation blandt diabetespatienter og rammer op til 25 % af denne befolkningsgruppe. Infektioner opstår ofte i disse sår (de tegner sig for 40 %-80 % af tilfældene) og fører til øget sygelighed og dødelighed. Diabetiske fodinfektioner (DFI'er) består normalt af polymikrobielle infektioner med en række identificerede anaerobe bakterielle patogener. Forskellige faktorer, herunder defekter i fibroblastfunktionen, problemer med kollagendannelse, cellulære immunmekanismer og fagocytfunktion, kan hæmme sårheling hos diabetespatienter. Flere undersøgelser har identificeret nedsat hudiltning som en stærk risikofaktor for amputationer relateret til DFI'er.
Som en af de nuværende muligheder for DFI-behandlingDet er rapporteret, at HBOT forbedrer helingsraten for diabetiske fodsår betydeligt, hvilket efterfølgende reducerer behovet for amputationer og komplicerede kirurgiske indgreb. Det minimerer ikke kun behovet for ressourcekrævende procedurer, såsom klapkirurgi og hudtransplantation, men giver også lavere omkostninger og minimale bivirkninger sammenlignet med kirurgiske muligheder. En undersøgelse foretaget af Chen et al. viste, at mere end 10 sessioner med HBOT førte til en forbedring på 78,3 % i sårhelingsraten hos diabetespatienter.
2. Nekrotiserende bløddelsinfektioner
Nekrotiserende bløddelsinfektioner (NSTI'er) er ofte polymikrobielle, typisk opstået fra en kombination af aerobe og anaerobe bakterielle patogener og er ofte forbundet med gasproduktion. Selvom NSTI'er er relativt sjældne, har de en høj dødelighed på grund af deres hurtige progression. Rettidig og passende diagnose og behandling er nøglen til at opnå gunstige resultater, og HBOT er blevet anbefalet som en supplerende metode til behandling af NSTI'er. Selvom der stadig er uenighed om brugen af HBOT ved NSTI'er på grund af manglen på prospektive kontrollerede studier,Beviser tyder på, at det kan være korreleret med forbedrede overlevelsesrater og organbevarelse hos NSTI-patienterEt retrospektivt studie indikerede en signifikant reduktion i dødeligheden blandt NSTI-patienter, der fik HBOT.
1.3 Infektioner på operationsstedet
SSI'er kan klassificeres baseret på infektionens anatomiske sted og kan opstå fra forskellige patogener, herunder både aerobe og anaerobe bakterier. Trods fremskridt inden for infektionskontrolforanstaltninger, såsom steriliseringsteknikker, brugen af profylaktiske antibiotika og forbedringer i kirurgisk praksis, er SSI'er fortsat en vedvarende komplikation.
En betydelig gennemgang har undersøgt effekten af HBOT i forebyggelsen af dybe SSI'er ved neuromuskulær skoliosekirurgi. Præoperativ HBOT kan reducere forekomsten af SSI'er betydeligt og fremme sårheling. Denne ikke-invasive behandling skaber et miljø, hvor iltniveauet i sårvævet er forhøjet, hvilket har været forbundet med den oxidative dræbende virkning mod patogener. Derudover adresserer den de lave blod- og iltniveauer, der bidrager til udviklingen af SSI'er. Ud over andre infektionskontrolstrategier er HBOT blevet anbefalet, især til rent kontaminerede operationer såsom kolorektale procedurer.
1.4 Forbrændinger
Forbrændinger er skader forårsaget af ekstrem varme, elektrisk strøm, kemikalier eller stråling og kan medføre høje sygeligheds- og dødelighedsrater. HBOT er gavnligt til behandling af forbrændinger ved at øge iltniveauet i beskadiget væv. Mens dyre- og kliniske studier viser blandede resultater vedrørendeEffektiviteten af HBOT i behandling af forbrændinger, en undersøgelse med 125 brandsårspatienter indikerede, at HBOT ikke viste nogen signifikant indvirkning på dødeligheden eller antallet af udførte operationer, men reducerede den gennemsnitlige helingstid (19,7 dage sammenlignet med 43,8 dage). Integration af HBOT med omfattende brandsårsbehandling kan effektivt kontrollere sepsis hos brandsårspatienter, hvilket fører til kortere helingstider og reduceret væskebehov. Yderligere omfattende prospektiv forskning er dog nødvendig for at bekræfte HBOTs rolle i behandlingen af omfattende forbrændinger.
1.5 Osteomyelitis
Osteomyelitis er en infektion i knogle eller knoglemarv, ofte forårsaget af bakterielle patogener. Behandling af osteomyelitis kan være udfordrende på grund af den relativt dårlige blodforsyning til knoglerne og den begrænsede penetration af antibiotika i marven. Kronisk osteomyelitis er karakteriseret ved vedvarende patogener, mild inflammation og nekrotisk dannelse af knoglevæv. Refraktær osteomyelitis refererer til kroniske knogleinfektioner, der fortsætter eller vender tilbage på trods af passende behandling.
HBOT har vist sig at forbedre iltniveauet i det inficerede knoglevæv betydeligt. Talrige case-serier og kohortestudier indikerer, at HBOT forbedrer de kliniske resultater for patienter med osteomyelitis. Det ser ud til at virke gennem forskellige mekanismer, herunder at øge metabolisk aktivitet, undertrykke bakterielle patogener, forbedre antibiotikas virkning, minimere inflammation og fremme heling.Efter HBOT viser 60 % til 85 % af patienter med kronisk, refraktær osteomyelitis tegn på infektionsundertrykkelse.
1.6 Svampeinfektioner
Globalt set lider over tre millioner individer af kroniske eller invasive svampeinfektioner, hvilket fører til over 600.000 dødsfald årligt. Behandlingsresultaterne for svampeinfektioner forringes ofte på grund af faktorer som ændret immunstatus, underliggende sygdomme og patogeners virulens. HBOT er ved at blive en attraktiv terapeutisk mulighed ved alvorlige svampeinfektioner på grund af dets sikkerhed og ikke-invasive natur. Undersøgelser tyder på, at HBOT kan være effektiv mod svampepatogener såsom Aspergillus og Mycobacterium tuberculosis.
HBOT fremmer svampedræbende virkninger ved at hæmme biofilmdannelsen af Aspergillus, med øget effektivitet observeret i stammer, der mangler superoxiddismutase (SOD) gener. De hypoksiske forhold under svampeinfektioner udgør udfordringer for tilførsel af svampedræbende lægemidler, hvilket gør de øgede iltniveauer fra HBOT til en potentielt gavnlig intervention, selvom yderligere forskning er berettiget.
De antimikrobielle egenskaber ved HBOT
Det hyperoksiske miljø, der skabes af HBOT, initierer fysiologiske og biokemiske ændringer, der stimulerer antibakterielle egenskaber, hvilket gør det til en effektiv supplerende behandling mod infektioner. HBOT udviser bemærkelsesværdige effekter mod aerobe bakterier og overvejende anaerobe bakterier gennem mekanismer som direkte bakteriedræbende aktivitet, forstærkning af immunresponser og synergistiske effekter med specifikke antimikrobielle midler.
2.1 Direkte antibakterielle virkninger af HBOT
Den direkte antibakterielle effekt af HBOT tilskrives i høj grad dannelsen af reaktive iltarter (ROS), som omfatter superoxidanioner, hydrogenperoxid, hydroxylradikaler og hydroxylioner - som alle opstår under cellulær metabolisme.
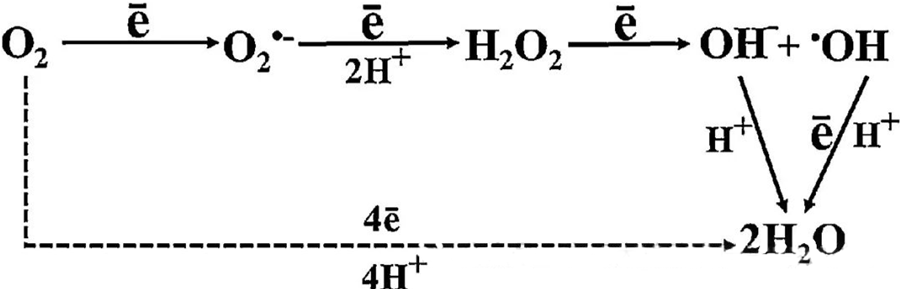
Interaktionen mellem O₂ og cellulære komponenter er afgørende for at forstå, hvordan ROS dannes i celler. Under visse betingelser, der kaldes oxidativ stress, forstyrres balancen mellem ROS-dannelse og nedbrydning, hvilket fører til forhøjede niveauer af ROS i cellerne. Produktionen af superoxid (O₂⁻) katalyseres af superoxiddismutase, som efterfølgende omdanner O₂⁻ til hydrogenperoxid (H₂O₂). Denne omdannelse forstærkes yderligere af Fenton-reaktionen, som oxiderer Fe²⁺ for at generere hydroxylradikaler (·OH) og Fe³⁺, hvorved en skadelig redoxsekvens af ROS-dannelse og cellulær skade initieres.
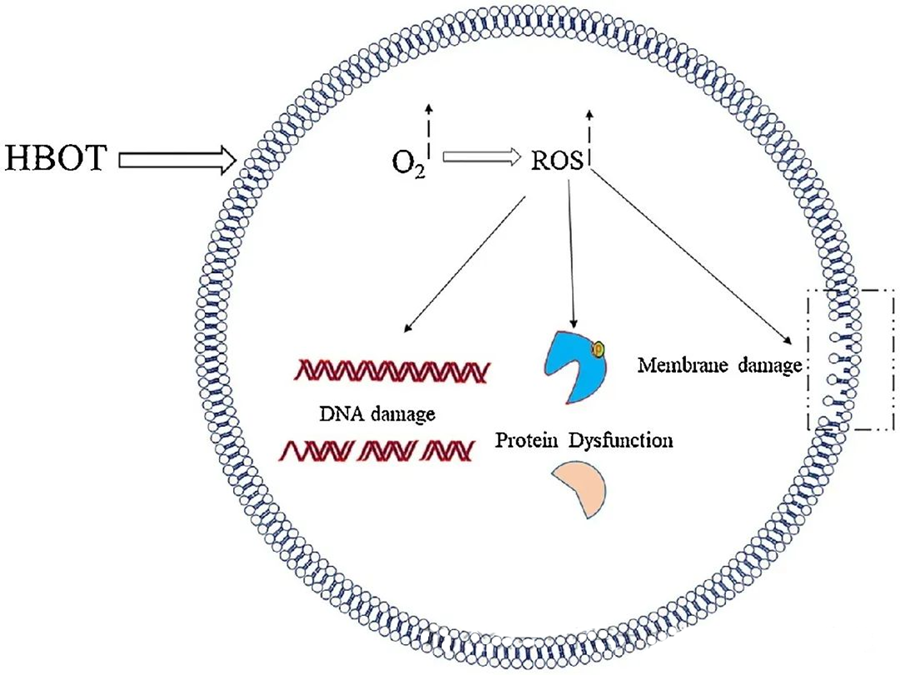
De toksiske virkninger af ROS er rettet mod kritiske cellulære komponenter såsom DNA, RNA, proteiner og lipider. Det er værd at bemærke, at DNA er et primært mål for H₂O₂-medieret cytotoksicitet, da det forstyrrer deoxyribosestrukturer og beskadiger basesammensætninger. Den fysiske skade induceret af ROS strækker sig til DNA'ets helixstruktur, potentielt som følge af lipidperoxidation udløst af ROS. Dette understreger de negative konsekvenser af forhøjede ROS-niveauer i biologiske systemer.
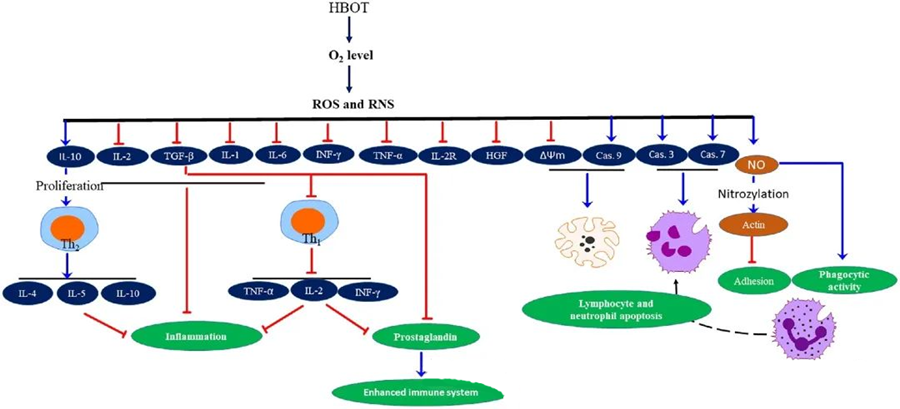
Antimikrobiel virkning af ROS
ROS spiller en afgørende rolle i at hæmme mikrobiel vækst, som det fremgår af HBOT-induceret ROS-generering. De toksiske virkninger af ROS er direkte rettet mod cellulære bestanddele som DNA, proteiner og lipider. Høje koncentrationer af aktive iltarter kan direkte beskadige lipider, hvilket fører til lipidperoxidation. Denne proces kompromitterer cellemembranernes integritet og dermed funktionaliteten af membranassocierede receptorer og proteiner.
Derudover undergår proteiner, som også er betydelige molekylære mål for ROS, specifikke oxidative modifikationer ved forskellige aminosyrerester såsom cystein, methionin, tyrosin, phenylalanin og tryptophan. For eksempel har HBOT vist sig at inducere oxidative ændringer i adskillige proteiner i E. coli, herunder elongationsfaktor G og DnaK, hvorved deres cellulære funktioner påvirkes.
Styrkelse af immunitet gennem HBOT
De antiinflammatoriske egenskaber ved HBOTer blevet dokumenteret, hvilket har vist sig afgørende for at lindre vævsskade og undertrykke infektionsprogression. HBOT påvirker signifikant ekspressionen af cytokiner og andre inflammatoriske regulatorer, hvilket påvirker immunresponset. Forskellige eksperimentelle systemer observerede forskellige ændringer i genekspression og proteingenerering efter HBOT, som enten opregulerer eller nedregulerer vækstfaktorer og cytokiner.
Under HBOT-processen udløser øgede O₂-niveauer en række cellulære reaktioner, såsom at undertrykke frigivelsen af proinflammatoriske mediatorer og fremme lymfocyt- og neutrofil-apoptose. Samlet set forstærker disse handlinger immunsystemets antimikrobielle mekanismer og letter dermed helingen af infektioner.
Desuden tyder studier på, at øgede O₂-niveauer under HBOT kan reducere ekspressionen af proinflammatoriske cytokiner, herunder interferon-gamma (IFN-γ), interleukin-1 (IL-1) og interleukin-6 (IL-6). Disse ændringer omfatter også nedregulering af forholdet mellem CD4:CD8 T-celler og modulering af andre opløselige receptorer, hvilket i sidste ende hæver interleukin-10 (IL-10) niveauerne, hvilket er afgørende for at modvirke inflammation og fremme heling.
HBOTs antimikrobielle aktiviteter er forbundet med komplekse biologiske mekanismer. Både superoxid og forhøjet tryk har vist sig inkonsekvent at fremme HBOT-induceret antibakteriel aktivitet og neutrofil-apoptose. Efter HBOT forstærker en markant stigning i iltniveauer neutrofilernes bakteriedræbende egenskaber, en essentiel komponent i immunresponset. Desuden undertrykker HBOT neutrofiladhæsion, som medieres af interaktionen mellem β-integriner på neutrofiler med intercellulære adhæsionsmolekyler (ICAM) på endotelceller. HBOT hæmmer aktiviteten af neutrofil β-2 integrin (Mac-1, CD11b/CD18) gennem en nitrogenoxid (NO)-medieret proces, hvilket bidrager til migrationen af neutrofiler til infektionsstedet.
Den præcise omlejring af cytoskelettet er nødvendig for, at neutrofiler effektivt kan fagocytere patogener. S-nitrosylering af actin har vist sig at stimulere actinpolymerisering, hvilket potentielt letter neutrofilers fagocytiske aktivitet efter HBOT-forbehandling. Desuden fremmer HBOT apoptose i humane T-cellelinjer gennem mitokondrielle signalveje, hvor der er rapporteret om accelereret lymfocytdød efter HBOT. Blokering af caspase-9 - uden at påvirke caspase-8 - har vist de immunmodulerende virkninger af HBOT.
De synergistiske effekter af HBOT med antimikrobielle midler
I kliniske anvendelser anvendes HBOT ofte sammen med antibiotika til effektivt at bekæmpe infektioner. Den hyperoxiske tilstand, der opnås under HBOT, kan påvirke virkningen af visse antibiotika. Forskning tyder på, at specifikke bakteriedræbende lægemidler, såsom β-laktamer, fluorquinoloner og aminoglykosider, ikke kun virker gennem iboende mekanismer, men også delvist er afhængige af bakteriers aerobe metabolisme. Derfor er tilstedeværelsen af ilt og patogeners metaboliske egenskaber afgørende, når man evaluerer antibiotikas terapeutiske virkninger.
Betydelig evidens har vist, at lave iltniveauer kan øge Pseudomonas aeruginosas resistens over for piperacillin/tazobactam, og at et miljø med lavt iltindhold også bidrager til den øgede resistens hos Enterobacter cloacae over for azithromycin. Omvendt kan visse hypoksiske tilstande øge bakteriel følsomhed over for tetracyklin-antibiotika. HBOT fungerer som en brugbar supplerende terapeutisk metode ved at inducere aerob metabolisme og reoxygenere hypoksisk inficerede væv, hvilket efterfølgende øger patogeners følsomhed over for antibiotika.
I prækliniske studier reducerede kombinationen af HBOT – administreret to gange dagligt i 8 timer ved 280 kPa – sammen med tobramycin (20 mg/kg/dag) signifikant bakteriemængden ved Staphylococcus aureus infektiøs endokarditis. Dette demonstrerer potentialet af HBOT som en supplerende behandling. Yderligere undersøgelser har vist, at HBOT under 37 °C og 3 ATA-tryk i 5 timer markant forstærkede virkningerne af imipenem mod makrofaginficerede Pseudomonas aeruginosa. Derudover viste den kombinerede modalitet af HBOT med cephazolin sig at være mere effektiv til behandling af Staphylococcus aureus osteomyelitis i dyremodeller sammenlignet med cephazolin alene.
HBOT øger også ciprofloxacins bakteriedræbende virkning signifikant mod Pseudomonas aeruginosa-biofilm, især efter 90 minutters eksponering. Denne forstærkning tilskrives dannelsen af endogene reaktive iltarter (ROS) og viser øget følsomhed i peroxidase-defekte mutanter.
I modeller af pleuritis forårsaget af methicillinresistente Staphylococcus aureus (MRSA) viste den samarbejdseffekt af vancomycin, teicoplanin og linezolid med HBOT signifikant øget effekt mod MRSA. Metronidazol, et antibiotikum, der i vid udstrækning anvendes til behandling af alvorlige anaerobe og polymikrobielle infektioner såsom diabetiske fodinfektioner (DFI'er) og infektioner i operationsstedet (SSI'er), har udvist højere antimikrobiel effektivitet under anaerobe forhold. Fremtidige undersøgelser er berettigede til at undersøge de synergistiske antibakterielle effekter af HBOT kombineret med metronidazol i både in vivo og in vitro-sammenhænge.
Den antimikrobielle effekt af HBOT på resistente bakterier
Med udviklingen og spredningen af resistente stammer mister traditionelle antibiotika ofte deres styrke over tid. Derudover kan HBOT vise sig at være essentiel i behandling og forebyggelse af infektioner forårsaget af multiresistente patogener og tjene som en kritisk strategi, når antibiotikabehandlinger mislykkes. Talrige undersøgelser har rapporteret de betydelige bakteriedræbende virkninger af HBOT på klinisk relevante resistente bakterier. For eksempel reducerede en 90-minutters HBOT-session ved 2 ATM væksten af MRSA væsentligt. Derudover har HBOT i ratiomodeller forstærket de antibakterielle virkninger af forskellige antibiotika mod MRSA-infektioner. Rapporter har bekræftet, at HBOT er effektiv til behandling af osteomyelitis forårsaget af OXA-48-producerende Klebsiella pneumoniae uden at kræve supplerende antibiotika.
Kort sagt repræsenterer hyperbarisk iltbehandling en alsidig tilgang til infektionskontrol, der forbedrer immunresponset og samtidig forstærker effekten af eksisterende antimikrobielle midler. Med omfattende forskning og udvikling har den potentiale til at afbøde virkningerne af antibiotikaresistens og giver håb i den igangværende kamp mod bakterieinfektioner.
Opslagstidspunkt: 28. feb. 2025

